
生(shēng)技新藥

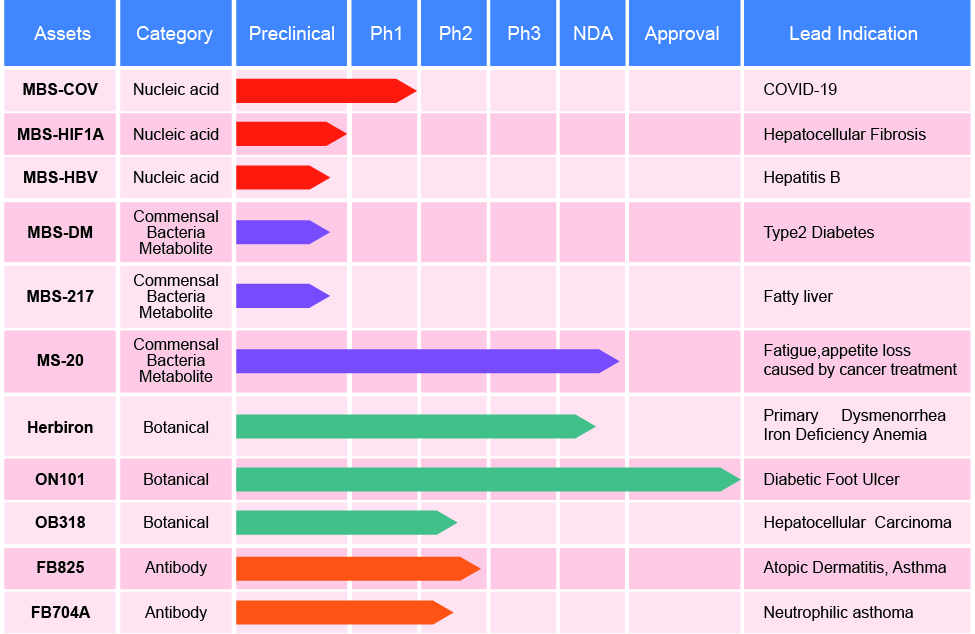
MBS-COV(SNS812)
适應症
冠狀病毒病
現況
1. 已完成MBS-COV臨床前藥理(lǐ)及毒理(lǐ)試驗,并成功合成cGMP藥物。
2. 已于2023年(nián)4月28日(rì)取得(de)美國(guó)一期臨床試驗結果,并于5月取得(de)最終臨床研究報告(Clinical study report, CSR)。
3. 于2023年(nián)5月31日(rì)向美國(guó)FDA提出二期臨床試驗申請(qǐng),并于6月9日(rì)向台灣TFDA提出多國(guó)多中心之二期臨床試驗申請(qǐng)。
産品優勢
目前市場上的疫苗與抗體(tǐ),針對病毒最易突變的棘蛋白(bái),容易被病毒逃脫,進而導緻疫苗突破(vaccine breakthrough)與疫情反複爆發。MBS-COV爲小核酸藥物,靶向病毒不易突變的位置,依據論文數據顯示可(kě)廣效抑制冠狀病毒。相(xiàng)關數據發表于國(guó)際醫學期刊EMBO Mol Med. 2022;14(4):e15298.
藥物機(jī)制
MBS-COV爲siRNA核酸藥物,利用RNA幹擾(RNA interference)機(jī)制,抑制病毒複制。
市場潛力
根據市場分(fēn)析機(jī)構的統計(jì),到2025年(nián),新冠預防市場将達到607億美元 (Reportlinker, OCT 2022); 到2031年(nián),預防市場将達到162億美元 (Transparency market research, FEB 2023)
化療漾MS20
适應症
改善癌症病患因化學治療所引起的疲勞及食欲不振
成分(fēn)
MS-20是大(dà)豆發酵代謝物的混合物,以微生(shēng)物模拟人(rén)體(tǐ)腸道環境經嚴格控制的發酵過程反應所産生(shēng)。
服用劑量與方式
每次服用4毫升,每日(rì)兩次分(fēn)别以溫開水100毫升稀釋後空腹食用。
現況
已于台灣地區上市
産品優勢
1.具改善腸道微生(shēng)态功能。
2.提升免疫,改善患者化療時之不良反應。
藥物機(jī)制
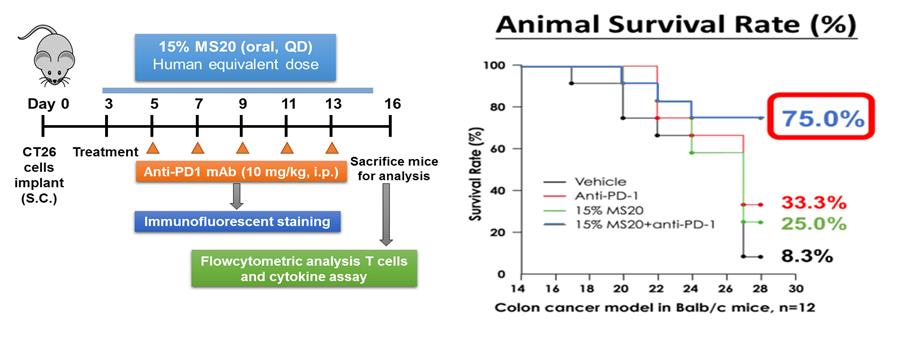
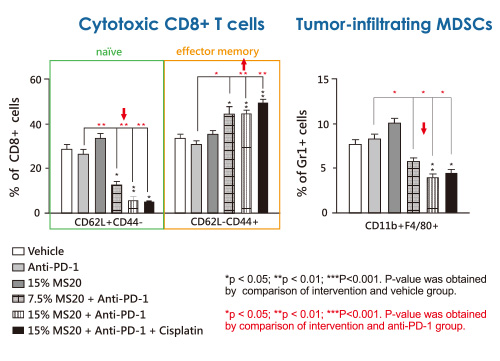
公司實驗數據顯示,MS20能改善受試者的腸道菌叢,增加菌種多樣性及豐富度,同時提升多種免疫細胞活性。此外,小鼠實驗數據還(hái)顯示,口服MS20可(kě)以提升罹癌小鼠對免疫檢查點藥物(anti-PD1)的反應率,罹癌小鼠的存活率提升超過2倍。
市場潛力
MS-20未來(lái)有機(jī)會合并應用于免疫檢查點藥物市場。根據知名分(fēn)析機(jī)構Market Data Forecast的預測,2019年(nián)免疫檢查點藥物市場已達129億美金,未來(lái)年(nián)複合成長高達28.68%,2024年(nián)的市場價值将到達454億美金。 (https://www.marketdataforecast.com/market-reports/global-checkpoint-inhibitors-market)
ON101
适應症
糖尿病足潰瘍。
現況
1.完成國(guó)際多中心三期臨床試驗(MRCT),ON101達顯著療效(16周完全愈合率爲60.7% vs. 35.1%, p=0.0001)。不同困難傷口完全愈合之次族群分(fēn)析,亦顯現ON101的療效顯著性。相(xiàng)關數據發表于國(guó)際醫學期刊JAMA Network Open(JAMA Network Open. 2021;4(9):e2122607)。
2.中國(guó)大(dà)陸、台灣、澳門(mén)、新加坡、馬來(lái)西亞新藥藥證核準;菲律賓、越南(nán)及印度尼西亞受理(lǐ)藥證審查。
3.美國(guó)FDA快(kuài)速審查認定,美國(guó)三期臨床試驗進行中。
2.中國(guó)大(dà)陸、台灣、澳門(mén)、新加坡、馬來(lái)西亞新藥藥證核準;菲律賓、越南(nán)及印度尼西亞受理(lǐ)藥證審查。
3.美國(guó)FDA快(kuài)速審查認定,美國(guó)三期臨床試驗進行中。
産品優勢
1.有效性:臨床試驗證實ON101對于傷口愈合具有顯著之療效并可(kě)減少疤痕的形成。
藥物機(jī)制
1.抑制發炎作(zuò)用
2.調節膠原蛋白(bái)生(shēng)成
3.促進損傷細胞的再生(shēng)能力
4.促進人(rén)類角質細胞增生(shēng)
2.調節膠原蛋白(bái)生(shēng)成
3.促進損傷細胞的再生(shēng)能力
4.促進人(rén)類角質細胞增生(shēng)
市場潛力
依據Fortune Business Insights的市場調查報告,糖尿病足潰瘍(DFU)的全球市場規模在2018年(nián)爲66億美元,年(nián)複合成長率爲6.8%,2026年(nián)市場預估約爲110億美元。
- ON101的植物萃取物、用途與制程技術(shù),已進行完整之全球專利布局,并取得(de)美國(guó)(發明專利,專利号US7985431B2、US8247004B2、US8449924B2、US9872879B2、US8105636B2、US10376488B2)、歐盟(發明專利,專利号1925310、2030626、2596798)、馬來(lái)西亞(發明專利,專利号MY-160153-A)、印度(發明專利,專利号263530)、日(rì)本(發明專利,專利号5086111、6290531)、中國(guó)(發明專利,專利号ZL 2007 1 0188280.3、ZL 2012 1 0128422.8)、韓國(guó)(發明專利,專利号10-0983754、10-1759751)與俄羅斯(發明專利,專利号2440819)專利,有效保護其智慧财産與技術(shù)。
- 合一生(shēng)技開發的糖尿病足部傷口潰瘍新藥ON101,目前已完成國(guó)際多中心三期臨床試驗(MRCT),經16周治療,療效顯著(完全愈合率爲62.2% vs. 34.7%(控制組), p=0.0001),與目前用藥Regranex相(xiàng)比,臨床數據更佳,可(kě)望在未來(lái)的糖尿病傷口愈合治療市場上創造價值。目前ON101已向藥監局提出Pre-NDA會議(yì)申請(qǐng),期待能早日(rì)上市并嘉惠衆多的糖尿病足潰瘍患者。
FB825
适應症
異位性皮膚炎、過敏性氣喘、高IgE症候群、食物過敏等過敏疾病。
産品優勢
1.特殊性:新穎作(zuò)用标的與作(zuò)用機(jī)制,抑制IgE的生(shēng)産源頭IgE B細胞。
2.安全性:藥理(lǐ)機(jī)制明确,副作(zuò)用低。
3.廣泛性:适應症寬廣,且可(kě)适用于更多的過敏和氣喘患者。
4.經濟性:FB825具有優異藥物動力學特性,能長時間在人(rén)體(tǐ)産生(shēng)作(zuò)用,預期能夠2~3個月用藥一次,長效作(zuò)用的優勢将大(dà)幅提高病患方便性以及醫療成本。
2.安全性:藥理(lǐ)機(jī)制明确,副作(zuò)用低。
3.廣泛性:适應症寬廣,且可(kě)适用于更多的過敏和氣喘患者。
4.經濟性:FB825具有優異藥物動力學特性,能長時間在人(rén)體(tǐ)産生(shēng)作(zuò)用,預期能夠2~3個月用藥一次,長效作(zuò)用的優勢将大(dà)幅提高病患方便性以及醫療成本。
現況
二期臨床試驗(哮喘)進行中
機(jī)制
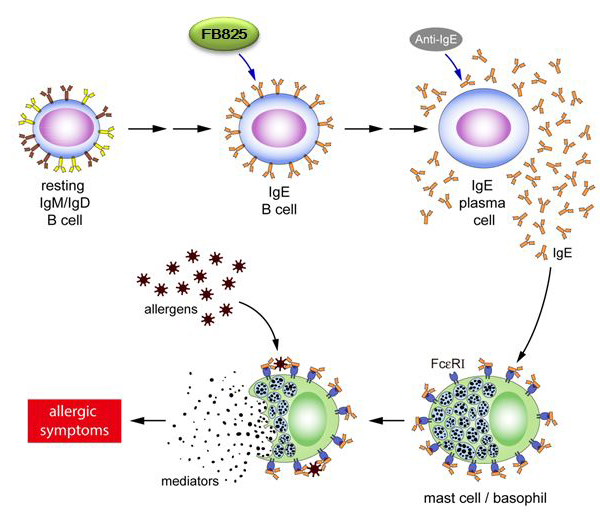
FB825爲拟人(rén)化的新一代IgG1單株抗體(tǐ)新藥,可(kě)與人(rén)體(tǐ)B細胞表面上IgE的CεmX片段結合,進而引起細胞毒殺反應,于前期直接封鎖會分(fēn)泌IgE 的B淋巴細胞,進而阻斷後續漿細胞(Plasma cell)的及IgE 的大(dà)量生(shēng)成,達成治療與預防過敏疾病的效果。
市場潛力
根據Allied Market Research與Coherent Market Insights分(fēn)析報告,異位性皮膚炎/哮喘治療全球市場将于2027年(nián)達380億美元。
- FB825已獲得(de)美國(guó)(發明專利,專利号US8460664B2、US8741294B2、US8974794B2)、歐盟(發明專利,專利号EP2401300B1)、日(rì)本(發明專利,專利号JP5848133B2、6068582)、中國(guó)(發明專利,專利号ZL201080009485.0、ZL201510069440.7)等主要制藥國(guó)專利核準,建立完整藥物、功效及抗原決定位之全球專利保護。
- FB825已完成美國(guó)一期臨床實驗,确認在人(rén)體(tǐ)上使用的安全性,並已在少樣本的探索性試驗中,證明藥物療效。目前美國(guó)人(rén)體(tǐ)二期試驗正加速進行,此外,FB825也獲得(de)美國(guó)FDA用于治療「高免疫球蛋白(bái)E症候群」(Hyper IgE Syndrome)的孤兒藥認定。
MBS-HIFA
适應症
癌症
産品優勢
1.靶點清楚,機(jī)制明确
2.藥效可(kě)長達3-6個月
3.HIF-1 alpha目前爲無藥靶點
4.核酸藥物合成快(kuài)速,開發成本低于抗體(tǐ)藥
5.易修飾并與其他(tā)藥物結合使用
2.藥效可(kě)長達3-6個月
3.HIF-1 alpha目前爲無藥靶點
4.核酸藥物合成快(kuài)速,開發成本低于抗體(tǐ)藥
5.易修飾并與其他(tā)藥物結合使用
現況
前臨床階段
機(jī)制
腫瘤由于生(shēng)長快(kuài)速,其内部環境容易形成缺氧,缺氧促使HIF-1 alpha蛋白(bái)活化。目前已知HIF-1 alpha的下遊路(lù)徑與腫瘤生(shēng)長、惡化、轉移與抗藥性息息相(xiàng)關,而有鑒于HIF-1 alpha路(lù)徑的重要性,其發現者也于2019年(nián)獲得(de)諾貝爾獎的殊榮。然而,雖然HIF-1 alpha相(xiàng)關的缺氧機(jī)制在許多腫瘤至關重要,至今卻無任何藥物成功上市。首先,HIF-1 alpha蛋白(bái)位于抗體(tǐ)藥物鞭長莫及的細胞内部,此外,HIF-1 alpha蛋白(bái)的結構表現尚無法找到小分(fēn)子藥物能有效結合的點位。換句話(huà)說(shuō),HIF-1 alpha是傳統藥物所難以觸及的靶點。MBS-HIF1A是能進入肝細胞,并專一性抑制HIF-1 alpha基因表現的藥物,能阻斷缺氧狀态下,HIF-1 alpha蛋白(bái)及其下遊基因對腫瘤的影(yǐng)響,進而達到腫瘤治療的目的。
市場潛力
目前已知所有腫瘤中,缺氧最嚴重的腫瘤分(fēn)别爲肝癌、胰髒癌與前列腺癌。一般體(tǐ)内氧氣濃度正常值都(dōu)在4%以上,低于1%就(jiù)會形成「病理(lǐ)性缺氧」并大(dà)幅活化HIF-1 alpha,而上述三種癌症的氧氣濃度達0.3~0.8%的病理(lǐ)性缺氧,因此這三種癌症都(dōu)可(kě)以是MBS-HIF1A優先靶向的适應症。肝癌、胰髒癌與前列腺癌目前都(dōu)是缺乏有效藥物的未滿足醫療缺口(Unmet medical need),潛在市場高達數十億美金。有鑒于中國(guó)肝癌每年(nián)新增病患已高達近50萬,成爲嚴重的醫療問(wèn)題,因此中天(上海)優先鎖定肝癌爲目标進行開發。
MBS-HBV
适應症
乙肝
産品優勢
1.靶點清楚,機(jī)制明确
2.藥效可(kě)長達3-6個月
3.國(guó)際研究已證實抑制病毒基因表現,達到乙肝功能性治愈的可(kě)行性
4.核酸藥物合成快(kuài)速,開發成本低于抗體(tǐ)藥
5.易修飾并與其他(tā)藥物結合使用
2.藥效可(kě)長達3-6個月
3.國(guó)際研究已證實抑制病毒基因表現,達到乙肝功能性治愈的可(kě)行性
4.核酸藥物合成快(kuài)速,開發成本低于抗體(tǐ)藥
5.易修飾并與其他(tā)藥物結合使用
現況
前臨床階段
機(jī)制
藉由靶向抑制乙肝病毒之重要關鍵基因,達到阻斷乙肝病毒蛋白(bái)對人(rén)體(tǐ)肝細胞的傷害,防止肝炎與繼發性肝癌的産生(shēng)。
市場潛力
根據統計(jì),中國(guó)的乙肝患者已高達總人(rén)口的7%,且85%的肝癌患者都(dōu)源自(zì)于乙肝(BMC Infectious Diseases vol. 19, Article number: 811, 2019)。然而上億乙肝患者中,積極接受治療的卻隻有200萬人(rén),潛在治療市場超過千億。治療率低的原因除了公衛知識尚未普及外,也與目前乙肝藥物隻能做到「部分(fēn)治愈(Partial cure)」相(xiàng)關。「部分(fēn)治愈」是指藥物隻能抑制病毒複制子代,卻無法抑制HBsAg等病毒抗原的持續表現,因此隻有在病毒複制子代的急性期,才會進行消極性的投藥治療。然而,許多時候,病毒雖不複制子代,但(dàn)長期持續表現的病毒蛋白(bái)(如(rú)S及X蛋白(bái))都(dōu)可(kě)能會使肝組織發生(shēng)病變。因此近幾年(nián)各國(guó)都(dōu)開始将「功能性治愈(Functional cure)」作(zuò)爲乙型治療的目标。「功能性治愈」指的是藥物能抑制病毒複制子代外,還(hái)能同時抑制病毒蛋白(bái)的表現,預防肝組織的進一步病變。MBS-HBV是中天(上海)自(zì)主研發,能從(cóng)源頭阻斷病毒蛋白(bái)表現,以達成「功能性治愈」爲目标的藥物。

